PUBLICIDADE
E se eu te dissesse que na patinação no gelo a pessoa patina sobre a água e não sobre o gelo? Isso pareceria um pouco estranho, não é mesmo?!
Porém, de certa forma, isso é o que de fato acontece. Para você entender melhor, veja o experimento abaixo, que pode ser usado em sala de aula a fim de explicar como a pressão influencia o ponto de fusão do gelo.
Materiais e reagentes:
- Uma barra de gelo que pode ser feita congelando água dentro de um pote pequeno de margarina;
- 50 cm de fio de náilon (linha de pesca);
- 2 pesos iguais (podem ser utilizadas duas garrafas de refrigerante de 2L cheias de água ou duas latas de refrigerante cheias de areia);
- 1 pedaço de madeira;
- 2 tijolos ou latas iguais.
Procedimento experimental:
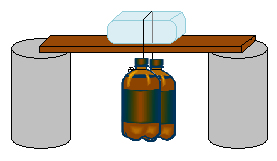
- Amarre cada um dos pesos numa extremidade do fio de náilon;
- Faça um suporte em que a madeira fique suspensa sobre os dois tijolos;
- Coloque o gelo sobre a madeira, no meio;
- Coloque o fio de náilon sobre o gelo, de modo que os pesos permaneçam suspensos e observe o que ocorre.
Resultados e Discussão:
Você observará que o fio de náilon cortará o gelo, atravessando-o. Porém, à medida que ele vai descendo e cortando o gelo, as partes acima do fio vão se congelando novamente.
Isso acontece porque a pressão exercida pelo peso faz com que o gelo derreta e o fio consegue, então, atravessá-lo. O gelo é menos denso do que a água, de modo que ao se aumentar a pressão, o volume diminui e o gelo passa para o estado líquido. Porém, a parte de água líquida que fica acima do fio volta a estar apenas sobre a pressão atmosférica e sua temperatura permanece abaixo de zero, voltando a congelar.
Em lugares cuja pressão atmosférica é maior, o ponto de fusão e de ebulição da água é maior também.
Esse processo de regelo explica o fato das geleiras conseguirem se movimentar de modo bem lento, à medida que as partes de baixo vão derretendo devido às pressões exercidas pelas camadas de gelo superiores.

Mas e a patinação no gelo? O que tem a ver com esse experimento?
Do mesmo modo que ocorreu nesse experimento, os patins de gelo possuem uma lâmina fina, que exerce uma grande pressão sobre a água congelada, fazendo-a derreter na faixa em que o patinador apoia o pé. Visto que o gelo derrete, o patinador consegue deslizar com maior facilidade. De fato, ele patina sobre a água!
Porém, não é devido apenas à pressão no peso do patinador sobre as lâminas dos patins que o gelo derrete. Pois, seria necessária uma pressão 120 vezes maior que a pressão atmosférica para diminuir o ponto de fusão do gelo em apenas 1ºC.

Então, por que o gelo da pista de patinação derrete?
Uma das teorias mais aceitas é que as moléculas que ficam na superfície do gelo interagem somente com as moléculas ao lado e abaixo delas, enquanto as que ficam abaixo da superfície interagem com moléculas em todo o redor. Desse modo, as moléculas da superfície estão como que mais “soltas” e podem passar para o estado líquido numa temperatura menor que o ponto de fusão do gelo.
Por Jennifer Fogaça
Graduado em Química






