PUBLICIDADE

Introdução:
Substância química ou apenas substância é um material que apresenta composição fixa e um conjunto de propriedades bem definidas e constantes.
Existem substâncias simples e compostas. Substâncias simples são aquelas com composição apenas de átomos ou moléculas de um mesmo elemento químico. Não é possível dividir uma substância simples em outras ainda mais simples. Alguns exemplos são:
H2, O2, O3, I2, N2, S8, os gases nobres (He, Ne, Ar, Kr, Xe, Rn), entre outros.
Já as substâncias compostas ou compostos químicos são formados por átomos (ou íons) de elementos químicos diferentes. Estes sim podem ser decompostos em outras substâncias mais simples ou compostas. Por exemplo, o hidróxido de sódio (NaOH) é composto de 3 elementos químicos diferentes, podendo ser dividido para obtermos outras substâncias como o gás hidrogênio, que é uma substância.
Esta é a proposta de texto: Realizar uma aula experimental para a obtenção do gás hidrogênio, por meio do hidróxido de sódio.
Aconselhamos que esse experimento seja feito pelo professor, pois necessita de certa cautela. Ele pode ser utilizado como auxílio no ensino do conteúdo de “Tipos de substâncias” e também no conteúdo da “Tabela Periódica”, como reconhecimento dos elementos químicos e suas propriedades.
Objetivo:
Obter uma substância simples (gás hidrogênio) e conhecer suas propriedades.
Materiais e Reagentes:
- Duas Pinças de madeira;
- Rolha de borracha;
- Dois tubos de ensaio de mesmo tamanho e proporções;
- Palitos de fósforo longos;
- Estante para tubos de ensaio;
- Lamparina ou Bico de Bunsen;
- Conta-gotas;
- Solução de hidróxido de sódio diluída;
- Papel de alumínio picado.
Procedimento Experimental:
Primeiro, são colocadas 10 gotas da solução de hidróxido de sódio em um dos tubos de ensaio, segurando-o com a pinça. Em seguida, adiciona-se ao sistema pedacinhos de papel alumínio e tampa-se imediatamente com a boca do outro tubo de ensaio; conforme mostrado abaixo:
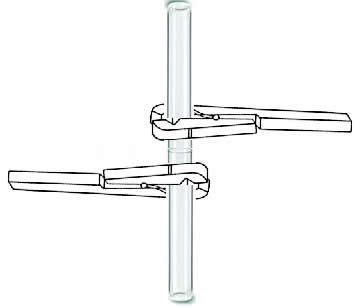
Espera-se mais de um minuto e guarda-se o tubo com o hidróxido e o alumínio na estante. O tubo da parte de cima deve ser tampado com a rolha rapidamente para não deixar o gás obtido escapar.
Posteriormente, a rolha é retirada e deve-se aproximar da boca do tubo de ensaio um palito de fósforo aceso.
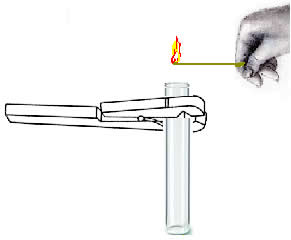
As observações devem ser anotadas.
Resultados e Discussão:
Com este experimento ocorre a seguinte reação entre o alumínio e o hidróxido de sódio:
2 NaOH + 2 Al + 2 H2O → 2 NaAlO2 + 3 ![]()
Entre os produtos formados, está o gás hidrogênio (H2) que é desprendido. Mas, no experimento, ele foi captado pelo outro tubo de ensaio. Dessa forma, obteve-se uma substância simples.
A função do palito de fósforo aceso foi iniciar a reação do hidrogênio com o oxigênio do ar, provando que o gás hidrogênio foi separado.
O professor pode discutir esses dados experimentais com os alunos.
Por Jennifer Fogaça
Graduada em Química
Equipe Brasil Escola





