A formação das estalactites e das estalagmites se dá da seguinte forma:
As águas subterrâneas possuem uma grande quantidade de gás carbônico (CO2) e de carbonato de cálcio (CaCO3) dissolvidos sob alta pressão.
CaCO3(s) + CO2(g) + H2O(l) →Ca2+(aq) + 2 HCO-3(aq)
Quando essa água goteja dentro das cavernas, onde a pressão é menor, ocorre a liberação do gás carbônico e a formação do carbonato de cálcio, que vai se depositando na forma de estalactites no teto e na forma de estalagmites no chão.
Ca2+(aq) + 2 HCO-3(aq)→CaCO3(s)+ CO2(g) + H2O(l)
O carbonato de cálcio é um sal inorgânico que está presente no mármore e no calcário e é usado na produção de vidro comum e de cimento para construções.
Em laboratório, é possível com um experimento bem simples formar estruturas semelhantes às estalactites e àsestalagmites. No lugar do carbonato de cálcio, outros sais inorgânicos podem ser usados, que são o bicarbonato de sódio (NaHCO3) e o sulfato de magnésio (MgSO4).
Esses sais são viáveis para este experimento porque podem ser encontrados facilmente em farmácias ou supermercados. O bicarbonato de sódio é muito usado como fermento de pães e bolos e como antiácido estomacal, já o sulfato de magnésio é mais conhecido como sal amargo ou sal de Epsom, sendo usado principalmente para aplicação medicinal devido à sua ação laxativa e também em massagens e banhos relaxantes.

Não pare agora... Tem mais depois da publicidade ;)
O professor pode realizar esse experimento com os alunos ao considerar o conteúdo de sais inorgânicos.
Materiais e Reagentes:
-
Bicarbonato de sódio (NaHCO3) ou sulfato de magnésio (MgSO4- sal amargo );
-
2 frascos vazios de papinha de neném;
-
2 arruelas (discos finos com um furo no meio usados normalmente para suportar a carga de um parafuso);
-
30 cm de fio grosso de lã ou de barbante de algodão;
-
1 pires;
-
1 colher.

Procedimento Experimental:
Coloque o sal até a metade dos dois fracos e adicione água até encher, misturando bem com a colher. Amarre as pontas do barbante em cada uma das duas arruelas e coloque-as submersas nas soluções. O pires deve ficar no meio dos dois frascos, abaixo do centro do fio, como mostra a figura a seguir:
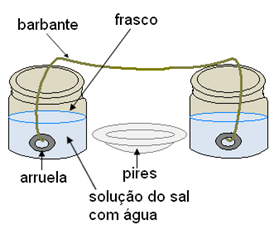
Deixe o sistema em repouso por cerca de três dias, em local que não ocorra trepidações e que seja bem arejado.
Resultados e Discussão:
Depois de passado o tempo de repouso, será observado a formação de estruturas bem parecidas com as estalactites no barbante e com as estalagmites no pires embaixo.
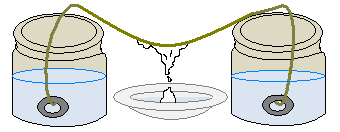
O professor pode então perguntar aos alunos como essas estruturas foram formadas, relacionando com a formação das estalactites e estalagmites nas cavernas.
Por Jennifer Fogaça
Graduada em Química










