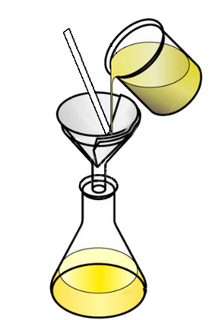
A atividade experimental que será explanada neste artigo tem como objetivo diferenciar as dispersões e identificá-las. Trata-se de uma prática bem simples, além de contar com materiais e reagentes de fácil obtenção.
Antes de realizá-la, o professor já deve ter abordado em sala de aula quais são os três tipos de dispersões (soluções (as partículas do soluto apresentam diâmetro menor que 1 nm), dispersões coloidais (entre 1 a 1000 nm) e suspensões (acima de 1000 nm)).
Outro ponto importante que também já deve ter sido mencionado para os alunos é que alguns coloides podem parecer a olho nu que são soluções, mas com o uso do microscópio, vemos que, na verdade, são heterogêneos, e não homogêneos, como uma solução verdadeira deve ser.
Existem vários métodos para realizar a determinação dos tipos de dispersões, mas a proposta deste artigo é fazer isso pela filtração comum realizada em laboratório. Esse procedimento baseia-se no princípio de que, para que a filtração das dispersões ocorra, é necessário que as partículas do soluto tenham um diâmetro acima de 1000 nm e fiquem retidas no filtro, separando-se do solvente. As dispersões coloidais (coloides) e as soluções verdadeiras não podem ter seus componentes separados por filtração.
Para realizar esta aula sobre determinação dos tipos de dispersões, você precisará dos seguintes materiais e reagentes:
- 6 béqueres;
- funil;
- papel de filtro;
- água;
- areia;
- amido de milho;
- sulfato de cobre II;
- tintura de iodo;
- microscópio (opcional).
* Procedimento Experimental:
1. Coloque a mesma quantidade de água nos três béqueres (encha aproximadamente até a metade);
2. Adicione 1 colher de sobremesa de areia no primeiro béquer, de amido de milho no segundo béquer e de sulfato de cobre II no terceiro béquer;
3. Misture bem as três dispersões e peça que os alunos anotem o aspecto observado em cada uma. Peça aos alunos que digam qual tipo de dispersão eles acreditam que seja cada uma;
4. Realize a filtração das três soluções, uma de cada vez, como mostra a figura inicial deste artigo e observe o que ocorreu;
5. Adicione tintura de iodo na solução filtrada de amido de milho para ver se ele foi filtrado ou não;
6. Se a escola tiver um microscópio, peça que os alunos observem por meio dele amostras das três soluções.
Não pare agora... Tem mais depois da publicidade ;)
7. Peça que digam se acertaram a ideia original que tinham sobre a classificação das três dispersões.
* Resultados e discussão:
Ao preparar as três soluções, os alunos poderão observar o seguinte:
- Béquer 1 (água + areia): trata-se de uma suspensão, pois a olho nu já fica claro que as partículas de areia não se dissolvem na água, mas formam uma mistura heterogênea, cujas partículas são tão grandes que as fases podem ser vistas;
- Béquer 2 (água + amido de milho): a dispersão fica branca, por isso, a olho nu, podem ocorrer confusões. Alguns podem achar que se trata de uma solução, tendo em vista que se observa apenas uma fase, e outros podem dizer que se trata de uma solução coloidal. Essa dúvida é tirada com o restante do experimento;
- Béquer 3 (água + sulfato de cobre II): a solução fica azul e totalmente homogênea. Isso ocorre porque o sulfato de cobre II (CuSO4(aq)) dissocia-se em água, formando os íons Cu2+ (que são responsáveis pela coloração azul) e SO42-. Os íons são partículas menores que 1 nm e nem mesmo através de um microscópio é possível ver os componentes separados, mas se observa uma mistura homogênea, portanto, trata-se de uma solução verdadeira.
Ao realizar a filtração, somente a dispersão do béquer 1 é totalmente separada, ficando a areia no papel de filtro e a água no béquer. Isso comprova que realmente se trata de uma suspensão.
No caso do béquer 2, a coloração branca diminui, o que pode levar alguns alunos a acharem que o amido de milho foi filtrado e trata-se de uma suspensão também. No entanto, é por isso que adicionamos a tintura de iodo no passo 5. O iodo na presença de uma dispersão de amido adquire tonalidade azul intensa, o que prova que não houve a separação pelo método da filtração e que a mistura água + amido é, na verdade, uma solução coloidal. Isso também pode ser comprovado quando se observa uma gota dessa dispersão em uma lâmina no microscópio.
Por fim, a mistura no béquer 3 não é separada pela filtração, mantendo os íons dissolvidos e, consequentemente, a coloração azul.
Por Jennifer Fogaça
Graduada em Química