Introdução:
A corrosão pode ser definida como o processo no qual o meio atua sobre determinado material e causa sua deterioração. Existem vários tipos de corrosão, mas a mais comum na natureza e em nosso cotidiano é a corrosão eletroquímica.
Esse é um processo espontâneo em que um metal entra em contato com um eletrólito e ocorrem reações de oxirredução, isto é, com transferência de elétrons, em que uma espécie química oxida (perde elétrons) e simultaneamente outra espécie química se reduz (ganha elétrons). A corrosão eletroquímica é caracterizada pela presença de água.
Um exemplo é a formação da ferrugem, que é o óxido de ferro (III) mono-hidratado (Fe2O3 . H2O), um composto que possui coloração castanho-avermelhada. A ferrugem se forma quando o ferro se oxida na presença de ar e água. Ocorre a oxidação do ferro metálico a cátion ferro:
Fe(s) → Fe2+ + 2e-
Simultaneamente, há a seguinte redução da água:
2H2O + 2e– → H2 + 2OH–
Ocorre a formação do hidróxido ferroso (Fe(OH)2), que na presença de oxigênio é oxidado a hidróxido de ferro III (Fe(OH)3). Posteriormente, ele perde água e se transforma no óxido de ferro (III) mono-hidratado (Fe2O3 . H2O), isto é, a ferrugem:
Fe2+ + 2OH– → Fe(OH)2
2Fe(OH)2 + H2O + 1/2O2 → 2 Fe(OH)3
2Fe(OH)3 → Fe2O3 . H2O + 2H2O
A aula experimental a seguir tem o objetivo de mostrar aos alunos um processo de identificação visual de reações de oxirredução, fazendo um estudo comparativo da corrosão do ferro por diversas substâncias.
Materiais e reagentes:
- 6 pregos;
- Barbante;
- Tesoura;
- 6 tubos de ensaio;
- Estante para tubos de ensaio;
- Água de torneira;
- Óleo de cozinha;
- Mistura de água e sal;
- Sabonete líquido ou mistura de sabonete com água;
- Água destilada;
- Caneta esferográfica.
Procedimento:
1. Enumere os tubos de ensaio de 1 a 6;
2. Coloque água da torneira no tubo 1, óleo no tubo 2, a mistura de água e sal no tubo 3, o sabonete líquido no tubo 4 e água destilada no tubo 5. Todos esses líquidos devem atingir cerca de ¼ do volume de cada tubo de ensaio. O sexto tubo deve ficar vazio.
3. Corte o barbante em 6 pedaços de cerca de 20 cm e prenda-os a cada um dos pregos;
4. Mergulhe cada prego em um líquido nos tubos de ensaio, deixando o barbante para fora de modo que seja possível puxar os pregos com os barbantes para tirá-los dos tubos;
5. Anote o aspecto dos pregos, dos líquidos e das soluções inicialmente;
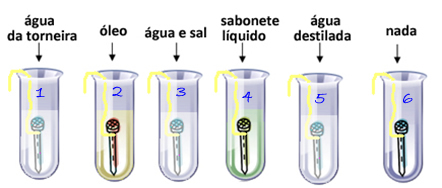
6. Deixe sete dias em repouso. Depois de passado esse tempo, observe novamente o aspecto dos líquidos e soluções e dos pregos.
Resultados e Discussão:
O professor pode pedir aos alunos que respondam o seguinte:
- Qual é a semiequação de oxidação do ferro e o seu número de oxidação (Nox)?
- Qual é a equação global de enferrujamento de um prego?
- Qual foi a ordem decrescente do meio mais agressivo para o meio menos agressivo para o prego? Por quê?
A ordem encontrada deve ser a seguinte:
Água com sal > água da torneira > água destilada > sabonete líquido > ar > óleo de cozinha.
Isso ocorre porque os principais componentes responsáveis pela formação da ferrugem são o oxigênio e a água. O óleo de cozinha impede o contato do ferro com o oxigênio do ar e, por isso, não há nenhuma mudança. Isso pode levar o professor a mostrar para os alunos que um método de proteção contra a corrosão do ferro é pintar o prego com uma tinta, impedindo que ele entre em contato com a água e o oxigênio.
O professor deve também chamar a atenção para a substância que se reduz. Na maioria dos casos, o oxigênio e a água são os que sofrem redução.
Por Jennifer Fogaça
Graduada em Química

