Uma pilha ou célula galvânica pode ser caracterizada como um processo espontâneo no qual a energia química é transformada em energia elétrica. Dessa forma, ela fornece energia para um determinado sistema até que a reação química se esgote. Essas reações são de oxirredução, de modo que envolve o fenômeno de transferência de elétrons.
Existem vários tipos de pilhas, sendo que a mais conhecida é a pilha seca de Leclanché. Existem também pilhas alcalinas, de mercúrio-zinco, de lítio-iodo e de níquel-cádmio. Esses tipos de pilhas são utilizados para fazer aparelhos elétricos funcionarem, como rádios, relógios, brinquedos e assim por diante.

Professor, você está transmitindo essa matéria para os seus alunos e quer um método que instigue a curiosidade deles, levando-os a observar os fenômenos de transferência de elétrons de um modo bastante interessante?
Então, o experimento a seguir é exatamente o que você procura. O melhor de tudo é que ele usará materiais de fácil obtenção e pode até mesmo ser apresentado numa Feira de Ciências da escola, juntamente com a abordagem de outros pontos referentes ao uso das pilhas, como seu descarte correto, reciclagem e uso atual pela sociedade.
Materiais e reagentes:
- Voltímetro (pode ser encontrado em lojas de material eletrônico ou de construção) ou uma lâmpada pequena de lanterna ou LED - Light Emitting Diode (Diodo Emissor de Luz), ou ainda, um relógio ou calculadora que funcionem com uma pilha comum de 1,5 V;
- 1 placa de cobre de aproximadamente 1,5 cm x 5 cm ou uma moeda de cobre (se você quiser um melhor resultado, utilize mais placas);
- 1 placa de zinco do mesmo tamanho que a anterior ou um prego de zinco;
- 2 fios elétricos de aproximadamente 40 cm cada com garras de jacaré (mostrado na figura abaixo, também encontrado em lojas de material eletrônico ou de construção);

- Palha de aço;
- Um limão (ou qualquer um dos seguintes: tomate, batata, laranja ou refrigerante de sabor cola).
Procedimento:
1. Limpe bem as duas placas metálicas de cobre e de zinco com a palha de aço;
2. Conecte os fios elétricos com as garras de jacaré em cada uma das placas de cobre e de zinco. Se você não conseguiu obter os fios elétricos com as garras de jacaré, faça o seguinte: Peque um prego e um martelo e faça um furo em uma extremidade da placa e ligue um fio comum de cobre às placas, passando no local do furo, como mostra a figura abaixo:
.jpg)
3. O fio elétrico deve estar conectado de um lado à placa e do outro ao voltímetro, ou lâmpada ou relógio. É importante que o fio não se encoste ao limão.
4. Pegue o limão (ou qualquer uma das frutas e verduras citadas) e faça dois pequenos cortes na casca, próximos da extremidade da fruta;
5. Espete as placas de metal no limão, tomando o cuidado para não tocá-las na casca, deixando os metais bem imersos no limão. O esquema deve ficar como o abaixo:
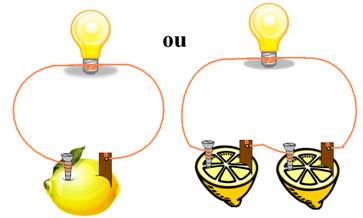
6. Observe o que acontece.
Resultados e Discussão:
Se você utilizar um voltímetro, ele irá marcar a voltagem da corrente elétrica, a lâmpada irá acender e o relógio ou a calculadora irão funcionar. Quanto mais limões você usar intercaladamente maior será a corrente elétrica produzida.

O limão é ácido e, portanto, em seu meio existem cátions H+ e também ânions, formando assim uma solução condutora de elétrons. O cobre atrai mais elétrons que o zinco, assim, ao colocarmos essas placas em contato por meio do fio de cobre, uma elevada quantidade de elétrons do zinco é transferida para o cobre.
Assim, as placas são os eletrodos e a solução ácida condutora é o eletrólito, que permite que essa reação ocorra continuamente. Também se pode utilizar como eletrólito soluções alcalinas e salinas. Por isso, que se utilizam o tomate (ácido), laranja (ácido), batata (alcalina) e o refrigerante de cola (que possui ácido fosfórico).
Por Jennifer Fogaça
Graduada em Química

