Artigos relacionados
Estratégias de ensino-aprendizagem
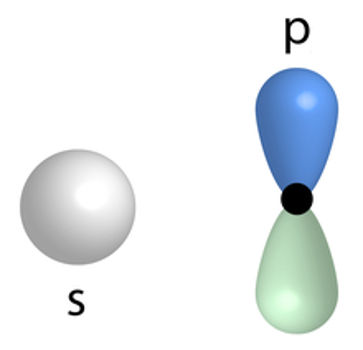
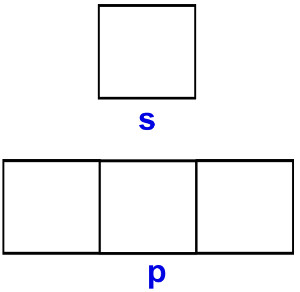
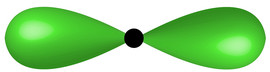
Como trabalhar ligações sigma e pi em sala de aula
Clique e conheça uma proposta pedagógica para trabalhar as ligações sigma e pi, de forma a envolver e melhorar o aprendizado em sala de aula.
Estratégias de ensino-aprendizagem
Construção de modelos para uma aula sobre geometria molecular
Prepare uma aula sobre geometria molecular a partir da construção de modelos pelos alunos para a visualização dos ângulos das ligações...
Estratégias de ensino-aprendizagem
O papel das atividades experimentais no ensino de Química
As práticas laboratoriais podem motivar a aprendizagem dos alunos?