Artigos relacionados
Estratégias de ensino-aprendizagem
Combustão completa e incompleta
Atividade experimental que demonstra a diferença entre elas.
Estratégias de ensino-aprendizagem
Combustão no Bico de Bunsen
Faça o teste da combustão completa e incompleta.
Estratégias de ensino-aprendizagem
Obtenção de substâncias simples – Hidrogênio
As substâncias simples são formadas por um mesmo tipo de elemento e podem ser obtidas a partir de substâncias compostas.
Estratégias de ensino-aprendizagem
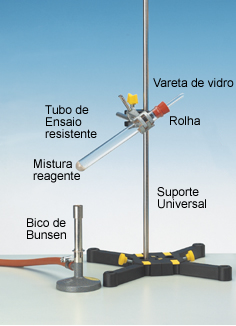
Produção de gás carbônico de forma experimental
Conheça uma estratégia de ensino para tratar de diversos assuntos da Química Inorgânica por meio da produção de gás carbônico de forma...